 |

 |









Một số người có thói quen uống một ly nước chanh ấm vào buổi sáng để thải độc gan, làm sạch cơ thể và giảm cân. Trong khi đó, dưới góc nhìn y học, gan vốn là cơ quan có chức năng tự giải độc cho cơ thể.

(GLO)- Sáng 28-5, Agribank Chi nhánh An Khê Đông Gia Lai đã tổ chức trao tặng kiosk y tế thông minh tiếp đón tự động cho Trung tâm Y tế Đak Pơ. Tham dự buổi lễ có đại diện Agribank Chi nhánh Đông Gia Lai, Agribank Chi nhánh An Khê Đông Gia Lai cùng lãnh đạo xã Đak Pơ.
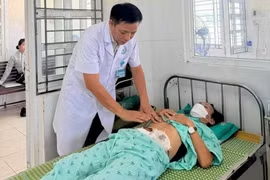
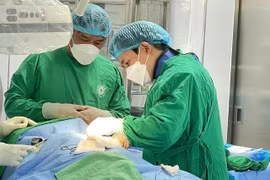
(GLO)- Các bác sĩ Bệnh viện Đa khoa Trung tâm tỉnh Gia Lai vừa phẫu thuật thành công cho bệnh nhân T.V.P (SN 1970, trú xã Phù Cát, tỉnh Gia Lai) mắc ung thư đại tràng sigma giai đoạn muộn với khối u kích thước lớn, xâm lấn nhiều cơ quan, nguy cơ biến chứng nặng.
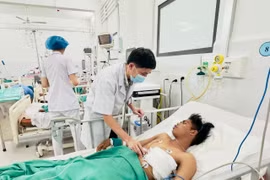
(GLO)- Ngày 26-5, Bệnh viện Đa khoa Gia Lai thông tin: Khoa Cấp cứu vừa tiếp nhận bệnh nhân Khuil (17 tuổi, làng O Đất, xã Ia Băng) nhập viện với vết thương thấu tim, tiên lượng tử vong cao. Đơn vị lập tức báo động đỏ nội viện, nhanh chóng xử trí cấp cứu góp phần cứu sống tính mạng người bệnh.

(GLO)- Từ ngày 1-4 đến nay, Bệnh viện Y dược cổ truyền và Phục hồi chức năng Pleiku (phường Pleiku, tỉnh Gia Lai), đã tầm soát loãng xương bằng dịch vụ kỹ thuật “Đo mật độ xương bằng máy siêu âm”miễn phí cho gần 100 bệnh nhân.
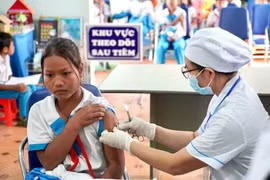
(GLO)- Theo quy định tại Nghị định 165/2026/NĐ-CP ngày 15-5-2026 hướng dẫn thi hành Luật Phòng bệnh, từ ngày 1-7, các cơ sở giáo dục mầm non và tiểu học sẽ phải thực hiện rà soát tiền sử tiêm chủng của học sinh ngay đầu năm học.

(GLO)- Theo thông tin từ Sở Y tế tỉnh Gia Lai, tính đến chiều 25-5, số nạn nhân trong vụ nghi ngộ độc thực phẩm liên quan đến bánh mì tại hộ kinh doanh Lâm Huyền (252 Hùng Vương, phường Quy Nhơn Đông) đã lên đến 75 người.

(GLO)- Ngày 25-5, lãnh đạo Bệnh viện Đa khoa Trung tâm tỉnh Gia Lai xác nhận: Đơn vị đang điều trị cho 39 trường hợp nghi ngộ độc thực phẩm sau khi ăn bánh mì mua tại một tiệm trên đường Hùng Vương (thuộc phường Quy Nhơn Đông).

(GLO)- Không chỉ mang hương thơm dịu nhẹ, hoa xoài còn được dân gian sử dụng như một vị thuốc tự nhiên, có tác dụng hỗ trợ tiêu hóa, thanh nhiệt, giảm viêm.

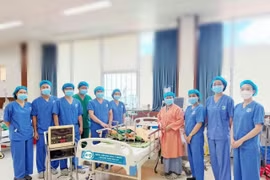

(GLO)- Chiều 22-5, tại xã Ia Dơk, Đoàn Kinh tế - Quốc phòng 74 (Binh đoàn 15) phối hợp với Bệnh viện Đa khoa Gia Lai tổ chức Ngày hội hiến máu tình nguyện.
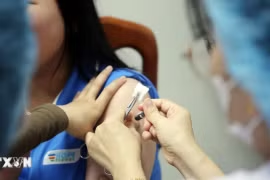
Một trong những nội dung đáng chú ý là quy định bệnh do virus HPV ở người thuộc danh mục bệnh phải sử dụng vaccine trong tiêm chủng bắt buộc thông qua hoạt động của Chương trình tiêm chủng mở rộng.

Táo và cam đều là trái cây giàu dinh dưỡng, phù hợp với chế độ ăn hỗ trợ kiểm soát đường huyết.

(GLO)- Theo Nghị quyết số 72-NQ/TW ngày 9-9-2025 của Bộ Chính trị về một số giải pháp đột phá, tăng cường bảo vệ, chăm sóc và nâng cao sức khỏe nhân dân, từ năm 2026, người dân được khám sức khỏe định kỳ hoặc khám sàng lọc miễn phí ít nhất mỗi năm 1 lần.

Điểm a khoản 1 Điều 14 Luật Dân số quy định trường hợp sinh con thứ hai, thời gian nghỉ thai sản đối với lao động nữ là 7 tháng; lao động nam là 10 ngày làm việc khi vợ sinh con.

(GLO)- Ủy ban nhân dân tỉnh Gia Lai vừa ban hành Kế hoạch triển khai hồ sơ bệnh án điện tử tại các cơ sở khám bệnh, chữa bệnh, với mục tiêu hoàn thành triển khai tại 100% cơ sở y tế trước ngày 31-12-2026.

Các nhà nghiên cứu cho biết sự kết hợp giữa bơ và xoài có thể giúp mạch máu giãn nở tốt hơn khi có dòng máu lưu thông - một dấu hiệu quan trọng phản ánh sức khỏe tim.

Gần một nửa người trưởng thành bị huyết áp cao, làm tăng nguy cơ đau tim và đột quỵ nguy hiểm.

(GLO)- Bộ Y tế vừa ban hành Thông tư 07/2026/TT-BYT quy định về tiêu chuẩn diện tích tại cơ sở khám - chữa bệnh, có hiệu lực từ ngày 1-6. Theo đó, đối với khu điều trị nội trú, phòng điều trị 1 giường phải bảo đảm diện tích tối thiểu 12 m²/giường, không bao gồm khu vệ sinh.



(GLO)- Theo UBND xã Hoài Ân, Đoàn công tác của Chương trình Phát triển Liên hợp quốc (UNDP) vừa có buổi làm việc và khảo sát thực địa tại Trạm Y tế cơ sở 4 xã Hoài Ân nhằm triển khai hạng mục xây dựng Trạm Y tế trong khuôn khổ Dự án “Làng Hòa bình Việt Nam - Hàn Quốc” (KVPVP) tại tỉnh Gia Lai.
(GLO)- Theo Trung tâm Kiểm soát bệnh tật tỉnh Gia Lai, trong tuần qua, toàn tỉnh ghi nhận 85 ca sốt xuất huyết Dengue (SXH) nâng tổng số ca mắc trên toàn tỉnh từ đầu năm 2026 đến nay lên 1.277 ca (tăng gần 500 ca so với cùng kỳ năm trước); không ghi nhận trường hợp tử vong do SXH.

(GLO)- Ngày 13-5, tại Sở Y tế tỉnh Gia Lai, đoàn kiểm tra liên ngành Trung ương số 4 đã có buổi làm việc với Ban Chỉ đạo liên ngành về an toàn thực phẩm (ATTP) tỉnh Gia Lai nhằm đánh giá công tác bảo đảm ATTP trên địa bàn tỉnh từ đầu năm đến nay.

(GLO)- Sầu riêng là loại trái cây được nhiều người yêu thích nhờ hương vị béo ngậy và giàu dinh dưỡng. Tuy nhiên, ăn quá nhiều, kết hợp sai thực phẩm hoặc dùng không đúng cách có thể gây đầy bụng, tăng đường huyết, nóng trong người và ảnh hưởng sức khỏe, đặc biệt với người có bệnh nền.

(GLO)- Ngày 12-5, đúng dịp kỷ niệm Ngày Quốc tế Điều dưỡng, Bệnh viện Nhi tỉnh Gia Lai (phường Pleiku) đã tổ chức thành công Hội thi Điều dưỡng và Kỹ thuật viên giỏi năm 2026. Hội thi diễn ra sôi nổi với sự tham gia của 46 thí sinh.

(GLO)- Ngày 13-5, tại phường Pleiku, Trung tâm Kiểm soát bệnh tật tỉnh Gia Lai tổ chức tập huấn nâng cao năng lực chuyên môn về phòng, chống tai nạn thương tích (TNTT) cho lãnh đạo và cán bộ chuyên trách 77 trạm Y tế các xã, phường khu vực phía Tây tỉnh.